
之前跟大家分享过《外泌体暗物质-DNA,真的存在吗?》,相信看过的同学们,已经初步了解了外泌体DNA的特征。那么近来外泌体DNA研究有哪些新进展呢?恩博先来给大家盘点一波:


转录因子FOXM1与细胞核中的MAP1LC3/LC3结合,FOXM1-chDNA(FOXM1结合的染色质基因或DNA片段),如DUX4基因和端粒DNA,通过FOXM1结合指定并转运到细胞质,然后在涉及LC3的溶酶体抑制期间通过分泌性自噬(SALI)释放到EVs。破坏FOXM1表达或SALI过 程会损害FOXM1-chDNA掺入EV。FOXM1-chDNA可以通过EVs传递到受体细胞,并在携带功能基因的受体细胞中表达。
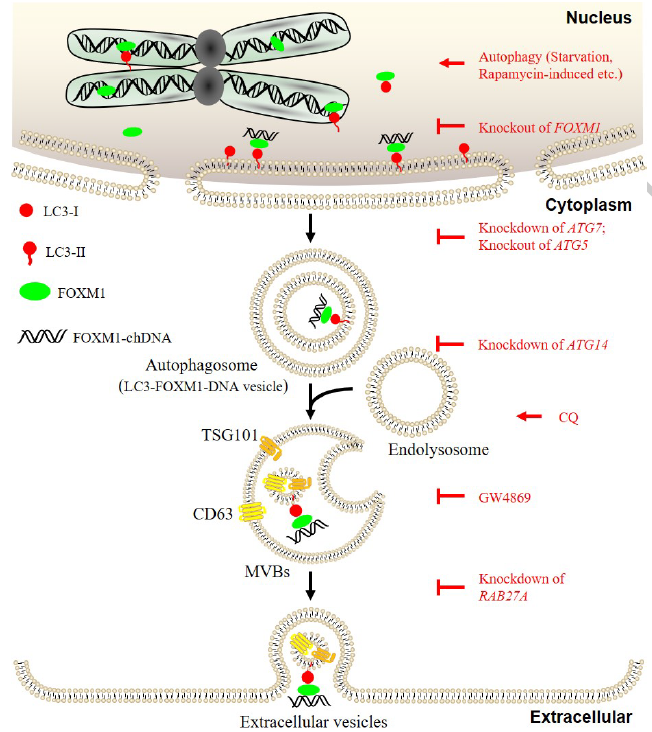
Ref:Transcription factor FOXM1 specifies chromatin DNA to extracellular vesicles. Autophagy. 2023 Nov 16. IF 13.3
线粒体DNA在有害刺激下从细胞中分泌的模式及其与人类疾病的相关性仍不清楚。焦亡细胞分泌包裹在外泌体中的mtDNA:Caspase-1的激活导致线粒体DNA通过gasdermin-D从线粒体泄漏到细胞质中,并诱导管腔内膜囊泡的形成,使mtDNA以外泌体形式分泌。mtDNA在外泌体内的包封促进了强烈的炎症反应,这种反应在体内外泌体生物合成抑制后得到改善。来自慢性全身炎症性疾病Behçet综合征(BS)患者的单核细胞显示出增强的Caspase-1激活,导致外泌体介导的mtDNA分泌和类似于BS患者的炎症病理。含有mtDNA的外泌体促进炎症,为人类炎症疾病中炎症的传播和恶化提供了新的见解。
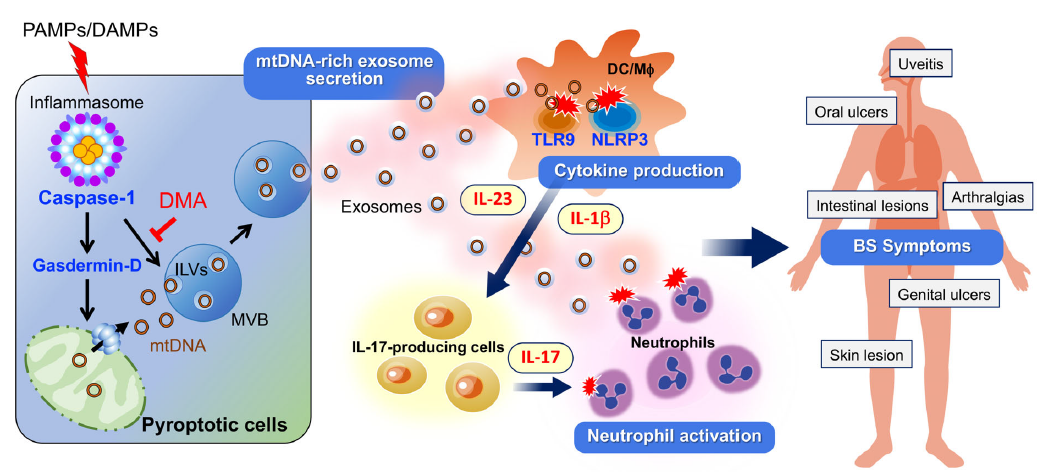
Ref:Secretion of mitochondrial DNA via exosomes promotes inflammation in Behçet's syndrome. EMBO J. 2023 Oct 16;42(20):e112573. IF 11.4
小细胞外囊泡(sEV)-DNA最近成为癌症诊断和预后的一种有前途的生物标志物,但其性质、负载机制、定位和脱落后功能相关的许多问题仍未得到解决。原子力显微镜(AFM)证实人髓性单核细胞白血病细胞MV4-11 sEV中EV染色质的存在。sEV dsDNA Pull down后蛋白质谱分析显示,30种蛋白质与EV-DNA相关,包括核心组蛋白如H2B和H4以及S100蛋白质。确定了涉及MDM2和S100蛋白(与EV染色质相关)的非突变p53失活是急性髓系白血病AML EV染色质调节BM-MSCs增殖的机制。相反,抑制MDM2或MDM2基因沉默,重新建立了BM-MSCs中p53靶点的表达。本研究揭示了AML和基质细胞之间通过EV染色质相互作用的新机制,这可能是AML治疗期间或治疗后造血衰竭的原因之一。
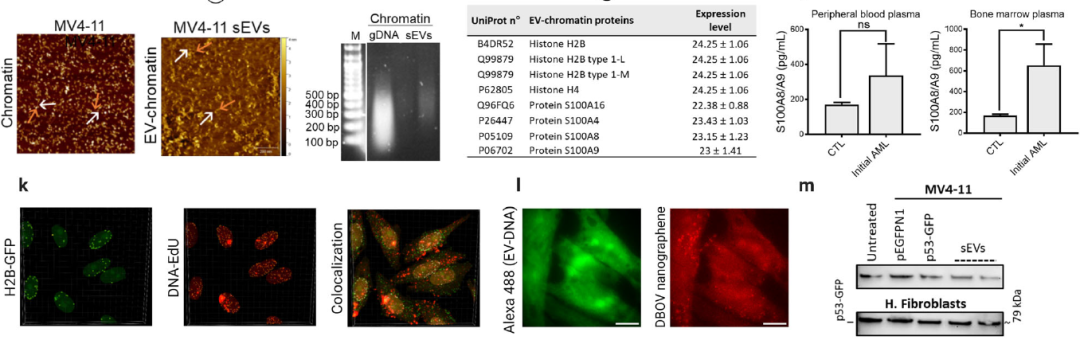
Ref:Extracellular vesicles transfer chromatin-like structures that induce non-mutational dysfunction of p53 in bone marrow stem cells. Cell Discov. 2023 Jan 31;9(1):12. IF 33.5
肺组织EVs通过递送双链DNA(dsDNA)促进骨髓中性粒细胞的趋化性。人类和小鼠肺组织分离的EVs含有dsDNA。结合肺组织EVs蛋白质组学和单细胞RNA测序数据分析表明,II型肺泡上皮细胞是肺组织EVs的主要来源。肺组织EVs在骨髓中积聚,在炎症条件下增强中性粒细胞的募集。肺组织EVs-DNA通过DNA-TLR9信号传导刺激中性粒细胞释放趋化因子CXCL1和CXCL2。
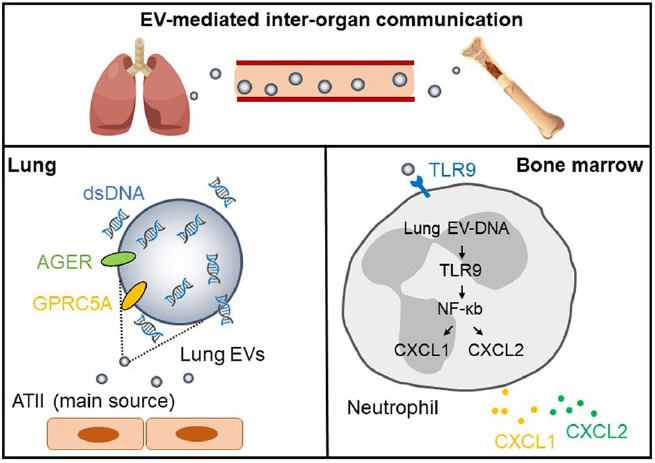
Ref:Extracellular
vesicles from lung tissue drive bone marrow neutrophil recruitment in
inflammation. J Extracell Vesicles. 2022 May;11(5):e12223. IF 16.0
从小鼠结肠炎和克罗恩病CD患者的血浆或结肠灌洗液中分离出EVs,外泌体dsDNA水平,包括mtDNA和nDNA,在小鼠结肠炎和活性人CD中显著增加,并与疾病活动度呈正相关。STING通路的激活在CD中得到了验证。来自活跃期人CD血浆的EVs和LPS损伤的结肠上皮细胞的EVs,显示出通过激活STING途径提高巨噬细胞的炎症,但在去除外泌体dsDNA后,这种作用消失了,STING缺乏可显著改善小鼠结肠炎。EVs释放抑制剂GW4869的应用通过抑制STING的激活成功地改善了小鼠结肠炎。总之,外泌体dsDNA通过激活巨噬细胞中的STING途径促进肠道炎症,并作为CD的潜在机制生物标志物和治疗靶点。详细解读链接:《合作成果|细胞外囊泡通过转运dsDNA激活肠道STING通路以加重克罗恩病炎症》。
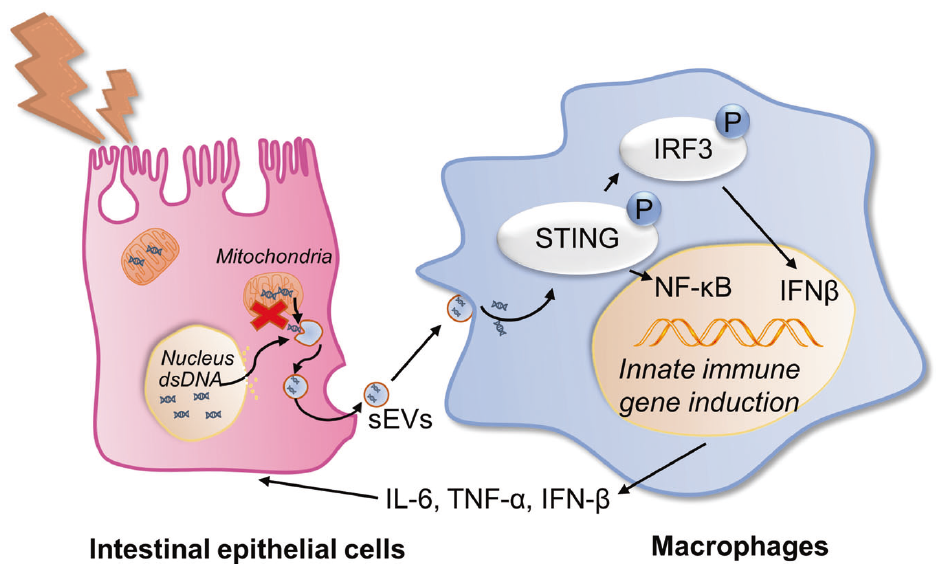
Ref:Extracellular vesicles package dsDNA to aggravate Crohn's disease by activating the STING pathway. Cell Death Dis. 2021 Aug 27;12(9):815. IF 9.0

采用ddPCR检测cfDNA和外泌体DNA(exoDNA)中KRAS突变,发现队列共计88例不同阶段胰腺导管腺癌PDAC患者和54例健康对照,验证队列包括39例PDAC患者和82例健康对照。在年龄匹配的对照组、局限性、局部晚期和转移性PDAC患者中,分别有7.4%、66.7%、80%和85%的外泌体DNA中存在KRAS突变。相比之下,在14.8%、45.5%、30.8%和57.9%的个体中检测到突变的KRAS cfDNA。较高的外泌体KRAS MAF与局部疾病患者的无病生存率下降有关。外泌体是肿瘤DNA的独特来源,可能与其他液体活检DNA互补。
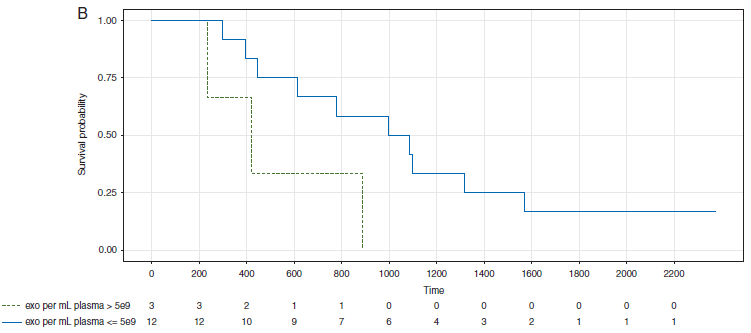

Ref:High prevalence of mutant KRAS in circulating exosome-derived DNA from early-stage pancreatic cancer patients. Ann Oncol. 2017 Apr 1;28(4):741-747. IF 50.5
基于SEC的方法从肾移植受者的尿液中富集纯化EV,尿液中evDNA占无细胞DNA(cfDNA)的29.2±8%。使用DNA酶处理和免疫胶体金电镜,证明evDNA与尿液EV/uEV表面结合。组织学正常(14例)、排斥损伤(10例)和非排斥损伤(16例)患者的正常evDNA产量和evDNA拷贝数显著不同,后一组的uEV粒径显著更大,uEV结合的DNA更多。供体来源DNA/ddDNA在肾移植受体的uEV样本中可检测到,但其数量变化很大。本研究支持应进一步研究evDNA作为同种异体肾损伤生物标志物的潜力。
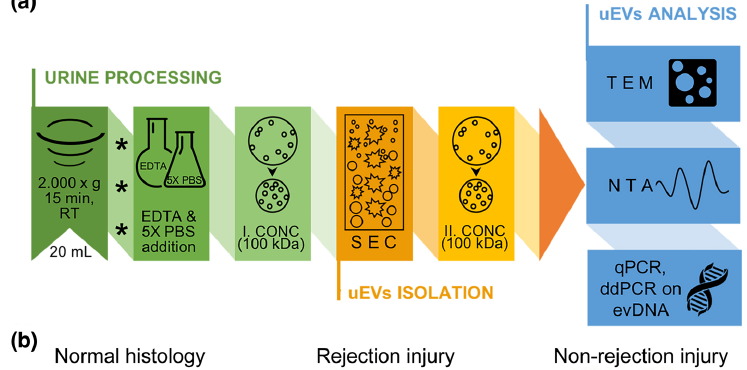
Ref:Extracellular vesicle-bound DNA in urine is indicative of kidney allograft injury. J Extracell Vesicles. 2022 Sep;11(9):e12268. IF 16.0
去分化脂肪肉瘤DDLPS患者或DDLPS细胞系的细胞外囊泡是MDM2 DNA 的载体,(16例DDLPS患者vs 6例健康对照血清EV,14个DDLPS组织vs 5例癌旁,提取DNA,探针法检测MDM2 CNV;引物设计在内含子区的PCR扩增证实了EV中MDM2 DNA的存在;DDLPS细胞系相对于脂肪前体细胞和LPS细胞系来源EV中含有更多MDM2 DNA)。ROC分析显示MDM2的曲线下面积(AUC)为95.8%,95%置信区间为86.9%至100%,表明DDLPS与健康对照之间存在稳健的分离。囊泡MDM2 DNA可以转移到脂肪前体细胞,脂肪前体细胞是DDLPS肿瘤微环境的主要和普遍存在的细胞成分,导致脂肪前体细胞中MDM2蛋白增加,影响下游通路:p53活性受损并增加基质金属蛋白酶2/MMP2产生、细胞增殖、迁移。
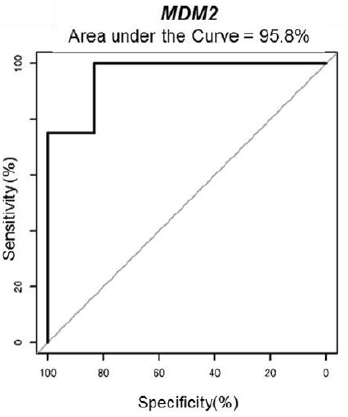
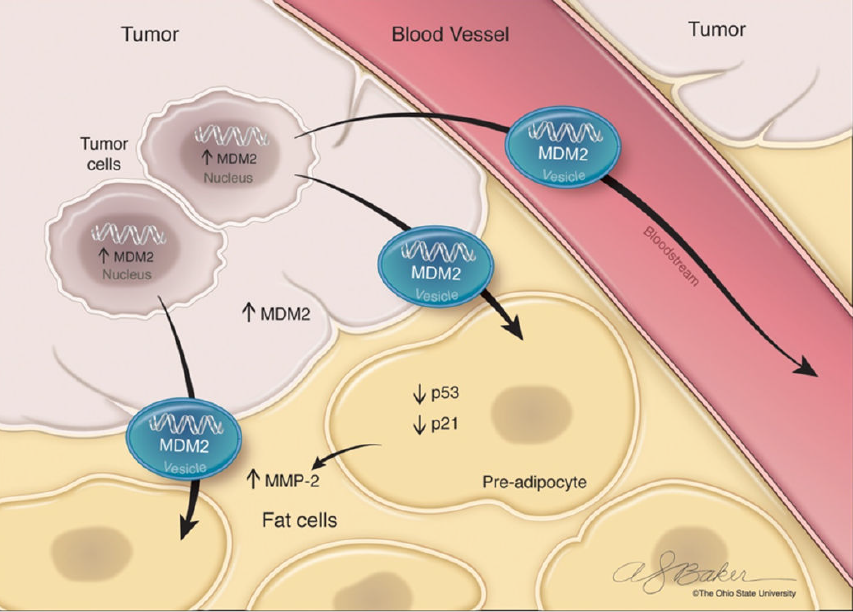
Ref:MDM2 Derived from Dedifferentiated Liposarcoma Extracellular Vesicles Induces MMP2 Production from Preadipocytes. Cancer Res. 2019 Oct 1;79(19):4911-4922. IF 11.2
嗜铬细胞瘤(PCC)和副神经节瘤(PGL)是最具遗传性的内分泌肿瘤。检测PCC和PGL中的体细胞突变对于基因诊断和术前评估仍然是不可行的。比较了患有PCC或PGL的患者或小鼠的血清外泌体DNA和肿瘤组织DNA,在患有PCC或PG L的患者的循环外泌体中发现了双链DNA(dsDNA)片段。外泌体dsDNA与母体肿瘤细胞的易感性基因具有相同的突变,PCC和PGL血清外泌体dsDNA与配对的肿瘤基因组高度一致。该发现为外泌体dsDNA的存在提供了第一个明确的证据,外泌体DNA可作为一种非侵入性遗传标记物,用于PCC和PGL的诊断和术前评估的最有效的体细胞突变筛查之一。
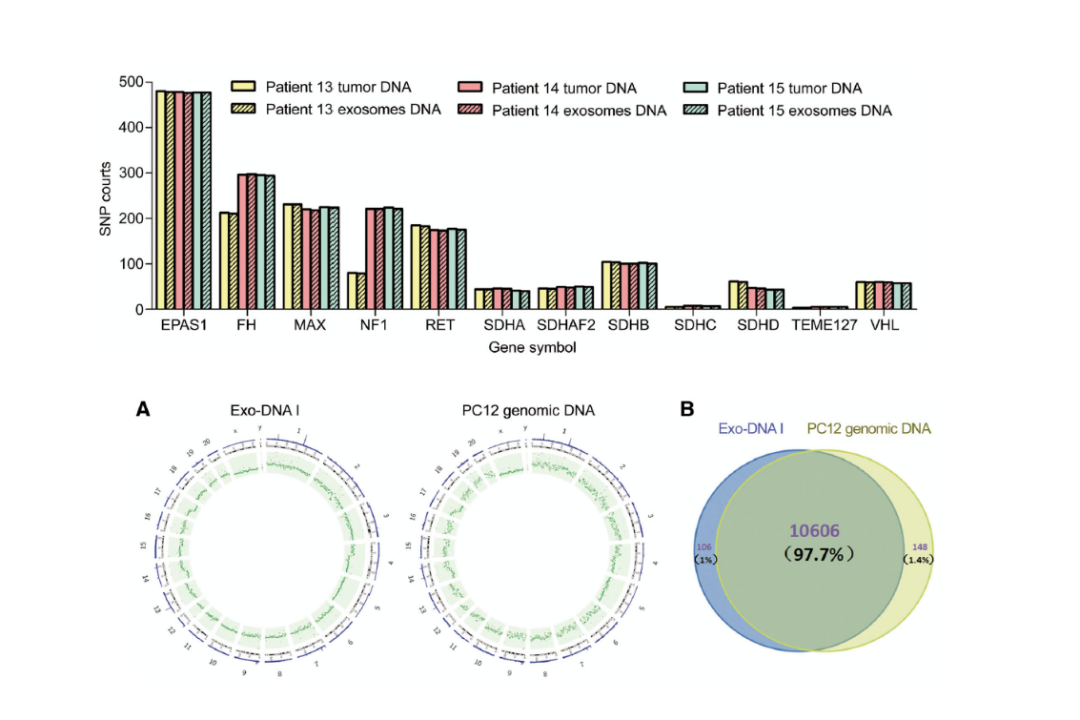
Ref:Exosomal double-stranded DNA as a biomarker for the diagnosis and preoperative assessment of pheochromocytoma and paraganglioma. Mol Cancer. 2018 Aug 23;17(1):128. IF 37.3
使用循环游离肿瘤DNA(cfDNA)的液体活检已成为检测突变的非侵入性选择;然而,许多患者循环中可检测的拷贝数太少,因此敏感性较低。作者开发并验证了一种新的测试方法,该方法通过同时捕获和检测外泌体RNA/DNA和cfDNA(exoNA),然后进行敏感的等位基因特异性qPCR,克服了突变拷贝丰度低无法检测的困难。活检证实T790M阳性(N=102)和T790M阴性(N=108)的NSCLC患者的血浆中提取ExoNA,T790M突变的敏感性为92%,特异性为89%。在胸内疾病(M0/M1a)患者中获得了高灵敏度(88%)。结论:与单独使用cfDNA的历史队列相比,外泌体RNA/DNA和cfDNA组合用于T790M检测具有更高的灵敏度和特异性。这可以进一步帮助避免T790M突变测试中不必要的肿瘤活检。
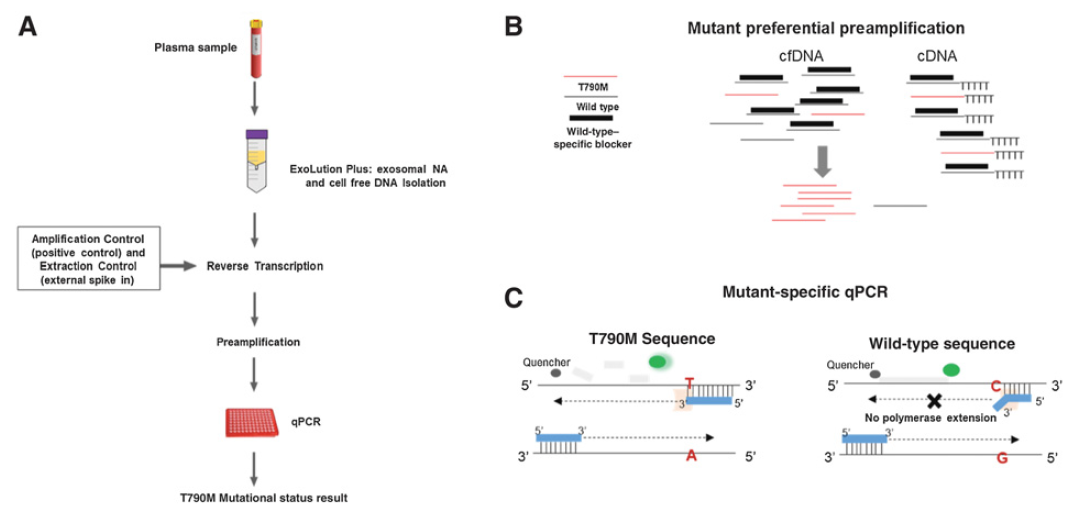
Ref:Exosome-Based Detection of EGFR T790M in Plasma from Non-Small Cell Lung Cancer Patients. Clin Cancer Res. 2018 Jun 15;24(12):2944-2950. IF 11.5


外泌体DNA建库方法和分析内容,与常规基因组DNA一样吗?当然不一样,容恩博卖个关子,有需求的扫码报名,即使不能获得资助名额,也能学习了解一下新技术不是?
上一篇 : “7”乐无穷 · 7载同庆| 钜惠狂享季